尚不清楚:肠道——大脑轴在双相中的作用机制:由于研究样本量小,疗效仍需更多临床试验验证。
之前看视频有说肠道-大脑轴对于自闭症的可能性,今天看一篇双相的基因组的已经发表的研究最后也提到了这个机制。
但是总体而言感觉还是不太可靠。需要进一步的研究证据和临床证据。
不过我个人对于双相不管是躁狂还是抑郁期,倾向于药物治疗,至少很多药物都已经是被明确验证过的,不管是对躁狂期的情绪稳定,还是抑郁期的抗抑郁,药物有它们明确的药理与作用机制。当然很讽刺的是,锂盐的稳定情绪的作用机制是也是不明的,但是它实证了对稳定情绪有用。
可惜一般的抗抑郁药物在用于治疗双相的抑郁时,会导致躁狂发作加重,或者其他副作用。但是抑郁期如果单纯服用锂盐做情绪稳定剂则往往不够。
尽管证据支持肠道-大脑轴在BD中的作用,但存在一些局限性,包括样本量较小(总样本量613名BD患者)、研究多为观察性设计,以及结果的不一致性(如具体微生物群变化差异)。这些限制表明需要更大规模的随机对照试验来确认疗效(Sublette et al., 2023)。
关键要点
研究表明,肠道-大脑轴可能在双相情感障碍(BD)中发挥重要作用,但具体机制仍需进一步探索。BD患者的肠道微生物群组成可能与健康人群不同,常见变化包括某些细菌的丰度增加或减少。益生菌、饮食干预和粪便微生物群移植等方法似乎可能改善BD症状,但效果尚有争议。
肠道-大脑轴简介
肠道-大脑轴是中枢神经系统与胃肠道之间的双向沟通网络,涉及神经、激素和免疫途径。研究建议,它可能通过影响大脑功能来参与BD的病理过程,比如通过调节炎症或神经递质。
BD中的微生物群变化
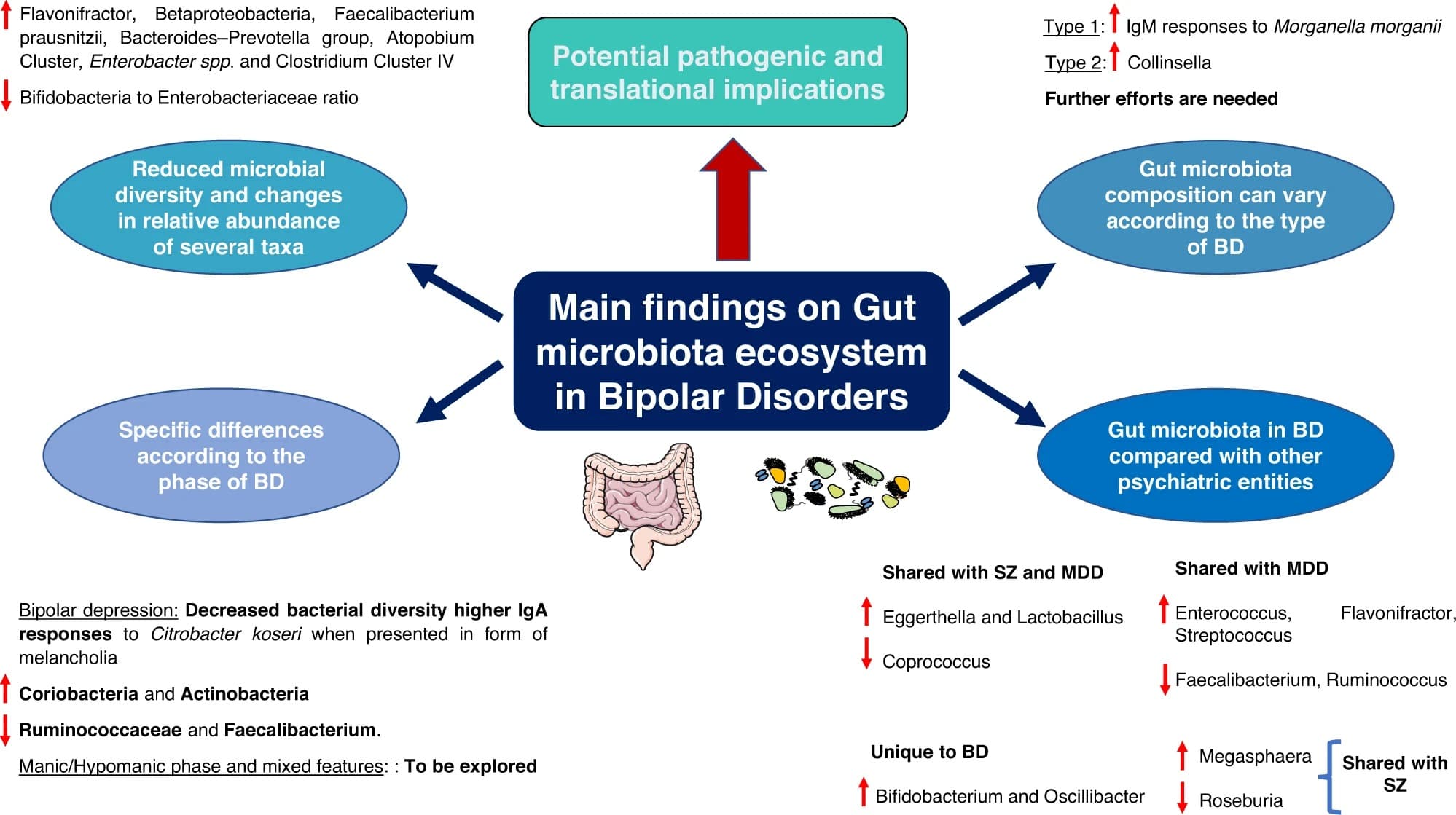
证据倾向于认为,BD患者的肠道微生物群与健康对照组存在差异。例如,Flavonifractor和Actinobacteria可能在BD患者中增加,而Ruminococcus和Faecalibacterium在健康人群中更常见。这些变化可能与BD的炎症状态和神经功能异常有关。
潜在治疗方法
研究显示,益生菌(如乳酸菌和双歧杆菌)可能减少BD患者的再住院率,并改善抑郁症状。地中海饮食和欧米伽-3脂肪酸也可能通过调节肠道微生物群改善症状。然而,由于研究样本量小,疗效仍需更多临床试验验证。
综述笔记:肠道-大脑轴在双相情感障碍中的潜在作用
引言
肠道-大脑轴(gut-brain axis)是指中枢神经系统(CNS)与胃肠道之间的双向沟通网络,涉及神经、激素和免疫途径。这一轴在维持体内稳态中起着关键作用,并与多种精神疾病(如抑郁症、焦虑症和双相情感障碍,BD)相关。BD是一种严重的慢性情绪障碍,表现为躁狂或轻躁狂与抑郁的交替发作,全球患病率约为1-3%。尽管治疗方法有所进步,但许多患者未能完全缓解,提示需要探索新的治疗途径。近年来的研究聚焦于肠道-大脑轴在BD病理生理学中的作用,表明调节肠道微生物群可能为治疗提供新方向。
BD中的肠道微生物群变化
多项研究发现,BD患者的肠道微生物群组成与健康对照组存在差异。一项2023年的系统综述分析了12项研究,涉及613名BD患者,发现患者肠道微生物群组成存在总体差异,乳酸菌(Lactobacillus)、粪便菌(Faecalibacterium)和瘤胃菌(Ruminococcus)的丰度变化最为常见,但具体变化因研究而异(A systematic review on gut–brain axis aberrations in bipolar disorder and methods of balancing the gut microbiota)。另一项2023年的综述进一步指出,BD患者表现出微生物多样性降低,特定菌群如Flavonifractor增加,而Faecalibacterium减少(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。2024年的一项研究聚焦于BD II型抑郁患者,发现促炎菌(如变形菌科、肠杆菌科)和与谷氨酸/GABA代谢相关的菌群(如双歧杆菌、拟杆菌)显著增加。这些变化可能与疾病的炎症状态和神经功能异常有关。
以下是BD中肠道微生物群变化的关键研究总结:
| 研究(年份) | 类型 | 参与者(BD患者) | 关键发现 |
|---|---|---|---|
| Coello et al. (2019) | 病例对照研究 | 113 | Flavonifractor在BD中更常见,61% vs. 39%健康对照 |
| Evans et al. (2017) | 病例对照研究 | 115 | Faecalibacterium在健康对照中更高 |
| Hu et al. (2019) | 病例对照研究 | 52 | 拟杆菌占主导,丁酸菌减少 |
| Painold et al. (2019) | 横断面研究 | 32 | 抑郁BD中Enterobacteriaceae增加,Actinobacteria和Coriobacteriaceae在BD中更高 |
| Aizawa et al. (2019) | 病例对照研究 | 39 | 双歧杆菌、乳酸菌无显著差异,与睡眠相关 |
| Lai et al. (2021) | 横断面研究 | 25 | 血浆色氨酸水平降低 |
| Bengesser et al. (2019) | 横断面研究 | 32 | 肠道菌多样性与ARNTL甲基化相关 |
| Eslami Shahrbabaki et al. (2020) | 随机双盲试验 | 38 | 益生菌降低抑郁和躁狂严重程度 |
| Reininghaus et al. (2020) | 队列研究 | 38 | 益生菌减少躁狂症状,改善认知功能 |
| Dickerson et al. (2018) | 随机对照试验 | 66 | 益生菌减少再住院率,改善症状 |
潜在机制
肠道微生物群通过多种途径影响大脑功能,包括短链脂肪酸(SCFAs)的产生、色氨酸-犬尿氨酸途径的调节以及免疫反应调控。这些机制可能导致BD的炎症状态和神经递质失衡:
短链脂肪酸(SCFAs):SCFAs(如丁酸)具有抗炎特性,可通过调节组蛋白去乙酰化酶影响大脑功能。研究发现,BD患者中丁酸产生菌(如Faecalibacterium)减少(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。色氨酸-犬尿氨酸途径:该途径在BD中发生改变,色氨酸及其代谢产物(如犬尿氨酸)水平降低,这对血清素合成至关重要。肠道微生物群在色氨酸代谢中起关键作用,失调可能加剧神经递质失衡(A systematic review on gut–brain axis aberrations in bipolar disorder and methods of balancing the gut microbiota)。免疫调节与炎症:肠道微生物群可影响全身和神经炎症,BD患者中促炎细胞因子(如IL-6、IL-8、TNF-α)水平升高,与特定微生物变化相关(The Microbiota–Gut–Brain Axis in Psychiatric Disorders)。BD患者常伴有肠道通透性增加,表现为更高水平的zonulin和claudin-5,与疾病早期发作和持续时间相关(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。HPA轴失调:肠道微生物群可影响下丘脑-垂体-肾上腺轴,BD患者中HPA轴失调导致异常的应激反应。
治疗意义
鉴于肠道微生物群与BD的关联,调节肠道-大脑轴被认为是潜在的辅助治疗策略。以下是一些关键干预措施:
益生菌:益生菌(如乳酸菌和双歧杆菌)显示出改善BD症状的潜力。一项研究发现,益生菌补充剂可减少再住院率并改善抑郁症状(Dickerson et al., 2018)。另一项研究表明,益生菌可改善认知功能和减少躁狂症状(Reininghaus et al., 2020)。饮食干预:富含纤维和欧米伽-3脂肪酸的饮食(如地中海饮食)与BD症状改善相关。欧米伽-3多不饱和脂肪酸(PUFAs)可改善抑郁症状,并可能通过调节肠道微生物群起作用(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。益生元:益生元促进有益菌的生长,被认为是管理BD症状的补充疗法。后生元:肠道细菌代谢产物(如SCFAs)在动物实验中显示出抗躁狂作用,可能通过表观遗传调控具有治疗潜力(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。抗菌药物:米诺环素等抗菌药物在BD抑郁阶段显示出疗效,可能通过改变肠道微生物群和减少炎症起作用(The microbiota-gut-brain axis and bipolar disorder)。粪便微生物群移植(FMT):一项案例报告显示,女性BD患者在接受9次FMT后6个月内无躁狂/抑郁症状,并减重33公斤(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。一项正在进行的临床试验(NCT03279224)评估FMT在BD抑郁中的疗效,监测24周后效果。免疫为基础的干预:塞来昔布对耐药性双相抑郁安全有效,减少焦虑,加速反应,但对细菌种群变化较小,无丁酸产生变化(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。N-乙酰半胱氨酸(NAC)在小鼠中缓解肠道失调和葡萄糖紊乱,可能对BD有益。
生活方式干预
运动:运动可增加有益细菌和微生物多样性,改善MGB轴功能(Microbiota–gut–brain axis mechanisms in the complex network of bipolar disorders: potential clinical implications and translational opportunities)。光疗和社会节奏疗法:异常光周期可改变Lactobacillus和Bacteroidetes丰度,光疗和社会节奏疗法可有益地修改肠道微生物群。季节性变化:季节性变化影响肠道微生物群(如夏季Actinobacteria增加,Firmicutes/Bacteroidetes比率增加),可能与BD发作相关。月经周期:月经周期可能影响BD情绪变化,estrobolome可能涉及,但目前无BD女性相关研究。
结论
肠道-大脑轴在BD的病理生理学中发挥重要作用,肠道微生物群的组成和功能变化可能导致炎症和神经递质失衡。通过益生菌、饮食干预、益生元和其他策略调节肠道-大脑轴为BD的辅助治疗提供了希望。然而,当前研究的局限性(如样本量小、观察性设计)表明需要更大规模的随机对照试验来确认这些发现。未来研究应聚焦于阐明具体机制,并开发针对性的肠道微生物群干预措施,以改善BD的临床管理。
关键引文
系统综述:肠道-大脑轴在双相情感障碍中的异常及其平衡方法综述:微生物群-肠道-大脑轴在双相情感障碍中的机制综述:微生物群-肠道-大脑轴在精神疾病中的作用综述:肠道-大脑轴与情绪障碍综述:微生物群-肠道-大脑轴在神经精神疾病中的作用综述:双相情感障碍与肠道微生物群的文献计量分析综述:肠道-大脑轴在神经系统疾病中的作用综述:肠道-大脑轴在精神健康障碍中的作用综述:微生物群-肠道-大脑轴与双相情感障碍